Alberto Papi*, Massimo Corradi*, Catherine Pigeon-Francisco, Roberta Baronio, Zenon Siergiejko, Stefano Petruzzelli, Leonardo M Fabbri†, Klaus F Rabe†
Lancet Respir Med 2013; 1: 23–31
*Joint first authors
†Senior authors
Σχεδιασμός Μελέτης
Σκοπός
Να διευρευνηθεί εάν το Foster® pMDI ως θεραπεία συντήρησης & ανακούφισης είναι πιο αποτελεσματικό από το Foster® pMDI ως θεραπεία συντήρησης και σαλβουταμόλη ως ανακουφιστική θεραπεία, σεασθενείς με μη-ελεγχόμενο άσθμα.
Σχεδιασμός
48-εβδομάδων, πολυεθνική, πολυκεντρική, διπλά-τυφλή, τυχαιοποιημένη, παράλληλων ομάδων, με ομάδα ενεργού ελέγχου.
Πληθυσμός ασθενών
1714 ενήλικες ασθενείς με:
- Διάγνωση άσθματος για τουλάχιστον 6 μήνες
- FEV1% τουλάχιστον 60% της προβλεπόμενης τιμής
- αύξηση του FEV1 κατά τουλάχιστον 12% και 200 ml μετά από εισπνοή 400μg σαλβουταμόλης
- προηγούμενη θεραπεία με ICS ή ICS/LABA
- τουλάχιστον μια σοβαρή παρόξυνση τους τελευταίους 12 μήνες (αλλά όχι τον τελευταίο μήνα)
- μη ελεγχόμενο άσθμα κατά τη διάρκεια του τελευταίου μήνα (δηλαδή τουλάχιστον ένα από τα ακόλουθα: χρήση ανακουφιστικής θεραπείας > δύο φορές την εβδομάδα, οποιονδήποτε περιορισμό δραστηριοτήτων, Οποιαδήποτε νυχτερινά συμπτώματα ή αφυπνίσεις, Ημερήσια συμπτώματα > δύο φορές την εβδομάδα, FEV1 < 80% της προβλεπόμενης τιμής)
Εισαγωγική περίοδος (run-in)
Όλοι οι ασθενείς έλαβαν Foster® pMDI 100/6 μg 1x2 και σαλβουταμόλη 100μg κατ’ επίκληση.
Θεραπείες
Εάν το άσθμα δεν ήταν πλήρως ελεγχόμενο μετά από την περίοδο run-in, οι ασθενείς συνέχισαν τη θεραπεία συντήρησης με Foster® pMDI 100/6μg 1x2 και τυχαιοποιήθηκαν ως εξής:

Πρωτεύον καταληκτικό σημείο
Βασικά ευρήματα από τη μελέτη
- H θεραπευτική προσέγγιση MART αύξησε σημαντικά τον χρόνο μέχρι την πρώτη σοβαρή παρόξυνση (πρωτεύον καταληκτικό σημείο)
Ο χρόνος μέχρι την πρώτη σοβαρή παρόξυνση αυξήθηκε κατά 75 ημέρες με τη θεραπευτική προσέγγιση MART συγκριτικά με Foster® + σαλβουταμόλη (209 ημέρες έναντι 134 ημερών, αντίστοιχα), με μια μείωση 36% του κινδύνου για σοβαρή παρόξυνση (12% έναντι 18% αντίστοιχα, hazard ratio 0.64, 95% CI 0.49-0.82, p=0.0005).
Χρόνος μέχρι την πρώτη σοβαρή παρόξυνση
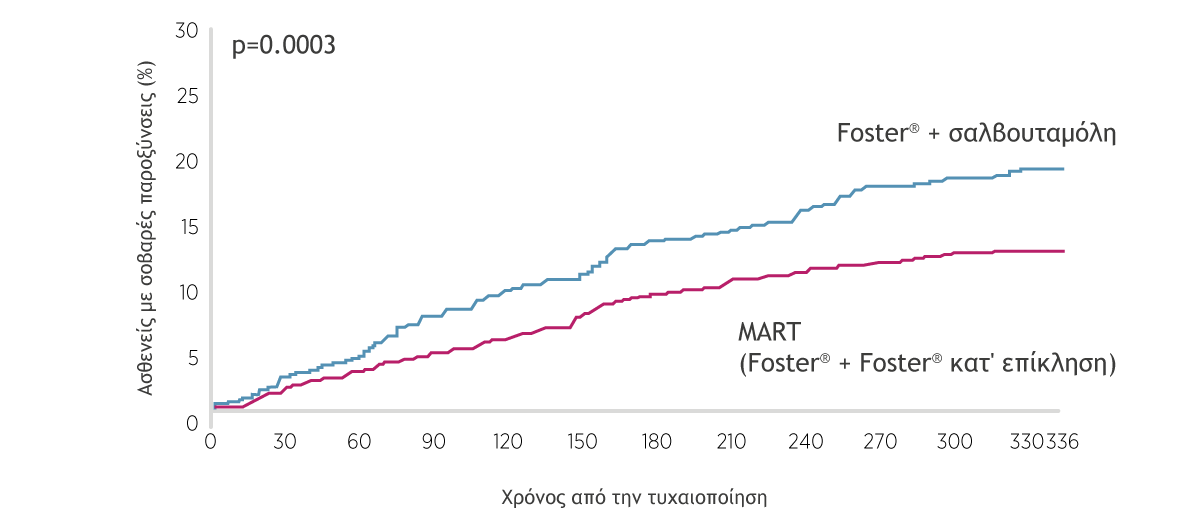
- Η MART μείωσε σημαντικά τον ετήσιο ρυθμό :
a. Των σοβαρών παροξύνσεων – 34% μείωση (14.76 στην τεχνική Foster® MART έναντι 22.39 Foster® + σαλβουταμόλη; hazard ratio 0.66, 95% CI 0.55-0.80, p<0.0001);
b. των επισκέψεων στα επείγοντα ή νοσηλειών – 33% μείωση (6.14 στην τεχνική Foster® MART έναντι 9.11 Foster® + σαλβουταμόλη; hazard ratio 0.67, 95% CI 0.54-0.84, p=0.0003);
c. της χρήση συστηματικών στεροειδών για >3 ημέρες – 35% μείωση (14.69 στην τεχνική Foster® MART έναντι 22.47 Foster® + σαλβουταμόλη; hazard ratio 0.65, 95% CI 0.54-0.80, p<0.0001).
Ετήσιος ρυθμός σοβαρών παροξύνσεων, χρήσης συστηματικών κορτικοστεροειδών, επισκέψεων στα επείγοντα/νοσηλείες
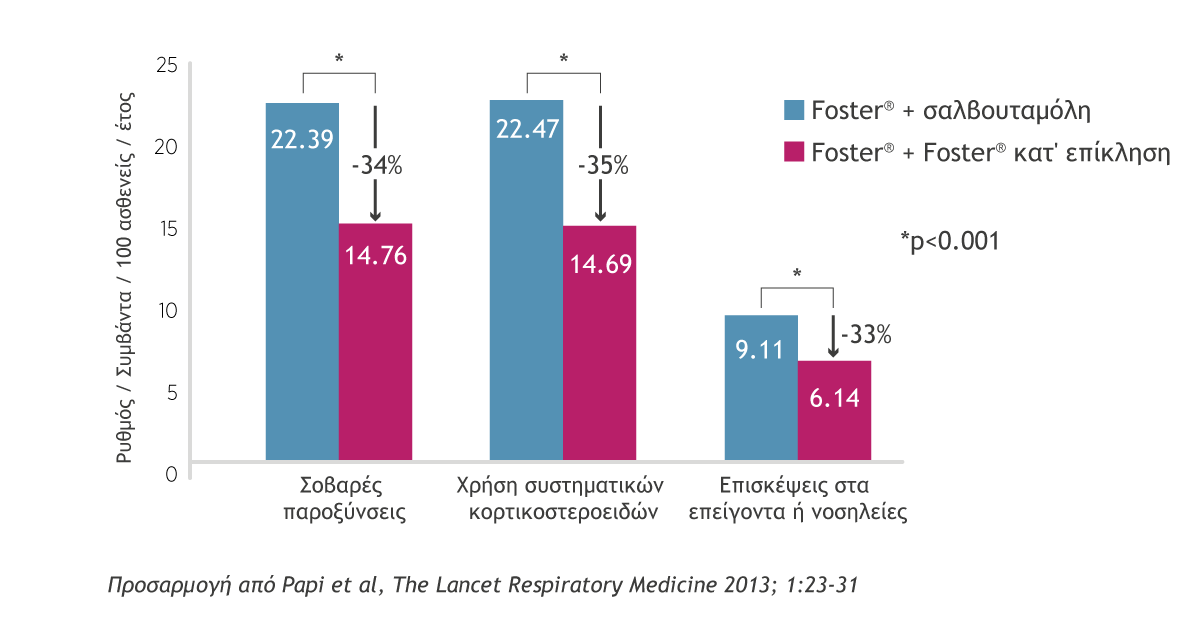
- Η MART μείωσε σημαντικά τον ρυθμό των ήπιων παροξύνσεων
Καμία σημαντική διαφορά μεταξύ των δύο ομάδων σχετικά με τον χρόνο μέχρι την πρώτη ήπια παρόξυνση. Όμως, ο ρυθμός των ήπιων παροξύνσεων μειώθηκε κατά 14% με τη MART (Foster® + Foster® κατ' επίκληση) συγκριτικά με Foster® + σαλβουταμόλη (56.04 έναντι 65.11, αντίστοιχα; hazard ration 0.86, 95% CI 0.76-0.98, p=0.021).
- Η MART βελτίωσε τις παραμέτρους της πνευμονικής λειτουργίας και του ελέγχου του άσθματος έναντι baseline χωρίς στατιστικά σημαντική διαφορά συγκριτικά με Foster® + σαλβουταμόλη
- Ο μέσος FEV1 βελτιώθηκε σε όλους τους ασθενείς κατά τη περίοδο run-in και επιπλέον βελτιώσεις καταγράφηκαν και στις δύο ομάδες κατά τη διάρκεια της μελέτης, με μια αλλαγή από το baseline μέχρι το τέλος της μελέτης κατά 0.090L και στις δύο ομάδες.
- Η μέση βαθμολογία των συμπτωμάτων στο άσθμα μειώθηκε σημαντικά από το baseline και στις δύο ομάδες χωρίς στατιστικά σημαντική διαφορά μεταξύ τους. Οι ημέρες ελεύθερες συμπτωμάτων (δηλαδή οι ημέρες χωρίς συμπτώματα ή χρήση ανακουφιστικής θεραπείας) αυξήθηκαν και στις δύο ομάδες χωρίς στατιστικά σημαντική διαφορά μεταξύ τους. H βελτίωση στο ερωτηματολόγιο ACQ-7 από το baseline ήταν ελαφρώς, αλλά όχι στατιστικά σημαντικά, μεγαλύτερη με τη MART θεραπευτική προσέγγιση (Foster® + Foster® κατ' επίκληση) συγκριτικά με Foster® + σαλβουταμόλη. Συνολικά, περίπου 50% των ασθενών με μη ελεγχόμενο άσθμα στο baseline (ACQ-7≥1.5) είχε μερικώς ελεγχόμενο άσθμα στο τέλος της μελέτης (ACQ-7<1.5).- Η μέση χρήση ανακουφιστικού φαρμάκου μειώθηκε σημαντικά από το baseline και στις δύο ομάδες (p<0.0001) χωρίς στατιστικά σημαντική διαφορά μεταξύ των δύο ομάδων.
MART (Maintenance And Reliever Therapy): Θεραπεία συντήρησης και ανακούφισης
Συχνή ερώτηση
- Ποιος είναι ο μέγιστος αριθμός κατ’ επίκληση εισπνοών Foster® 100/6 που μπορεί να λάβει ένας ασθενής με τη θεραπευτική προσέγγιση MART;
Στη θεραπευτική προσέγγιση MART, οι ασθενείς πρέπει να λαμβάνουν την ημερήσια δόση συντήρησης με Foster® 100/6μg με ημερήσια δόση 1 εισπνοή δύο φορές ημερησίως.
Επιπλέον, οι ασθενείς μπορούν να λάβουν κατ’ επίκληση ανακουφιστική θεραπεία για την αντιμετώπιση των συμπτωμάτων τους. Η μέγιστη ημερήσια δόση είναι 8 εισπνοές, δηλαδή 2 εισπνοές ως θεραπεία συντήρησης και μέγιστο 6 εισπνοές ως θεραπεία ανακούφισης. Εάν ένας ασθενής χρειάζεται συχνή χρήση ανακουφιστικής θεραπείας, συστήνεται αυστηρά να αναζητήσει ιατρική συμβουλή για την επαναξιολόγηση της κλινικής του κατάστασης.
Σοβαρή παρόξυνση ορίστηκε η επιδείνωση στο άσθμα που έχει ως αποτέλεσμα τη νοσηλεία ή την επίσκεψη στο τμήμα επειγόντων περιστατικών, ή ανάγκη λήψης συστηματικών κορτικοστεροειδών για τουλάχιστον 3 ημέρες.
Ήπια παρόξυνση ορίστηκε η εμφάνιση ενός από τα ακόλουθα: χρήση δύο ή περισσότερων εισπνοών κατ’ επίκληση ανακουφιστικού φαρμάκου επιπλέον από το baseline σε 24 ώρες, μείωση της πρωινής PEF κατά τουλάχιστον 20% από το baseline ή νυχτερινές αφυπνίσεις λόγω του άσθματος.

Περίληψη προφίλ ασφάλειας Foster® NEXThaler® 100/6:
Η πλέον συνήθης ανεπιθύμητη ενέργεια είναι ο τρόμος. Σε μια κλινική μελέτη 12 εβδομάδων με Foster® NEXThaler®, ο τρόμος παρατηρήθηκε μόνον με την υψηλότερη δοσολογία (2 εισπνοές δις ημερησίως), εμφανίστηκε συχνότερα κατά την έναρξη της θεραπείας και ήταν ήπιας έντασης. Κανένας ασθενής δεν αποσύρθηκε από τη μελέτη λόγω του τρόμου. Μεταξύ των ανεπιθύμητων ενεργειών που παρατηρήθηκαν, εκείνες που τυπικά συνδέονται με τη φορμοτερόλη είναι: τρόμος, κεφαλαλγία, ταχυκαρδία, κολπική βραδυκαρδία, στηθάγχη, ισχαιμία μυοκαρδίου, επιμήκυνση του διαστήματος QT. Μεταξύ των ανεπιθύμητων ενεργειών που παρατηρήθηκαν, αυτές που τυπικά συνδέονται με τη διπροπιονική βεκλομεθαζόνη είναι: ρινοφαρυγγίτιδα, καντιντίαση του στόματος, δυσφωνία, ερεθισμός του λαιμού, ευερεθιστότητα, μειωμένη ελεύθερη κορτιζόλη στα ούρα, μειωμένη κορτιζόλη στο αίμα, αυξημένη γλυκόζη στο αίμα. Όπως και με άλλες εισπνεόμενες θεραπείες, μπορεί να εμφανιστεί μετά τη χορήγηση της δόσης παράδοξος βρογχόσπασμος με άμεση αύξηση του συριγμού, του βήχα και της δύσπνοιας. To Foster® NEXThaler® αντενδεικνύεται σε ιστορικό υπερευαισθησίας στις δραστικές ουσίες ή σε κάποιο από τα έκδοχα του. Για περισσότερες πληροφορίες για τις ανεπιθύμητες ενέργειες του Foster® NEXThaler® συμβουλευτείτε την Περίληψη Χαρακτηριστικών Προϊόντος του Φαρμάκου2.
Περίληψη Προφίλ Ασφάλειας Foster® 100/6:
Όπως και με άλλες εισπνεόμενες θεραπείες, μπορεί να εμφανιστεί παράδοξος βρογχόσπασμος. Μεταξύ των ανεπιθύμητων ενεργειών που παρατηρήθηκαν, εκείνες που συνήθως σχετίζονται με τη φορμοτερόλη είναι: υποκαλιαιμία, κεφαλαλγία, τρόμος, αίσθημα παλμών, βήχας, μυϊκοί σπασμοί και επιμήκυνση του διαστήματος QTc. Οι ανεπιθύμητες ενέργειες που συνήθως σχετίζονται με τη διπροπιονική βεκλομεθαζόνη είναι: μυκητιασικές λοιμώξεις της στοματικής κοιλότητας, καντιντίαση του στόματος, δυσφωνία και ερεθισμός του λαιμού. Το Foster® αντενδεικνύεται σε υπερευαισθησία στη διπροπιονική βεκλομεθαζόνη, τη διυδρική φουμαρική φορμοτερόλη ή σε κάποιο από τα έκδοχα. Για περισσότερες πληροφορίες για τις ανεπιθύμητες ενέργειες του Foster® συμβουλευτείτε την Περίληψη Χαρακτηριστικών Προϊόντος του Φαρμάκου3.
Βιβλιογραφία
1. Papi A,et Al. The Lancet Respiratory Medicine 2013; 1:23-31
2. ΠΧΠ Foster® NEXThaler® 100/6
3. ΠΧΠ Foster® 100/6






Διαμοιρασμός περιεχομένου